Un pequeño gran avance en la lucha contra la peste porcina africana

La Peste Porcina Africana (PPA) es una enfermedad hemorrágica altamente infecciosa que afecta a cerdos domésticos y jabalíes europeos, provocando enormes pérdidas económicas en los países afectados. La PPA es una enfermedad de declaración obligatoria a la Organización Mundial de Sanidad Animal (OIE) y está provocada por el Virus de la Peste Porcina Africana (VPPA), virus de gran tamaño y complejidad contra el que aún no existe tratamiento ni vacuna eficaz.
Aunque la PPA suene exótica o lejana, desafortunadamente no lo es tanto. Así, el VPPA estuvo campando ininterrumpidamente durante casi 40 años por la Península Ibérica, desde su entrada inicial a través de Portugal en 1957 procedente del continente africano, causando estragos en la cabaña porcina y en el comercio porcino español. Si bien el VPPA inicialmente provocaba una PPA aguda caracterizada por una sintomatología muy clara y acompañada de una elevada mortalidad, con el paso de los años fueron apareciendo formas menos virulentas del VPPA que provocaban una enfermedad con tasas de mortalidad mucho más bajas y que dificultaba su detección y erradicación, favoreciendo la aparición de animales portadores asintomáticos y el establecimiento del virus en nuestro país de forma endémica. El perfeccionamiento de los métodos de diagnóstico junto con campañas de erradicación muy costosas, permitió la erradicación de la PPA en 1995, permitiendo la reapertura de las fronteras del comercio español a productos derivados del porcino.
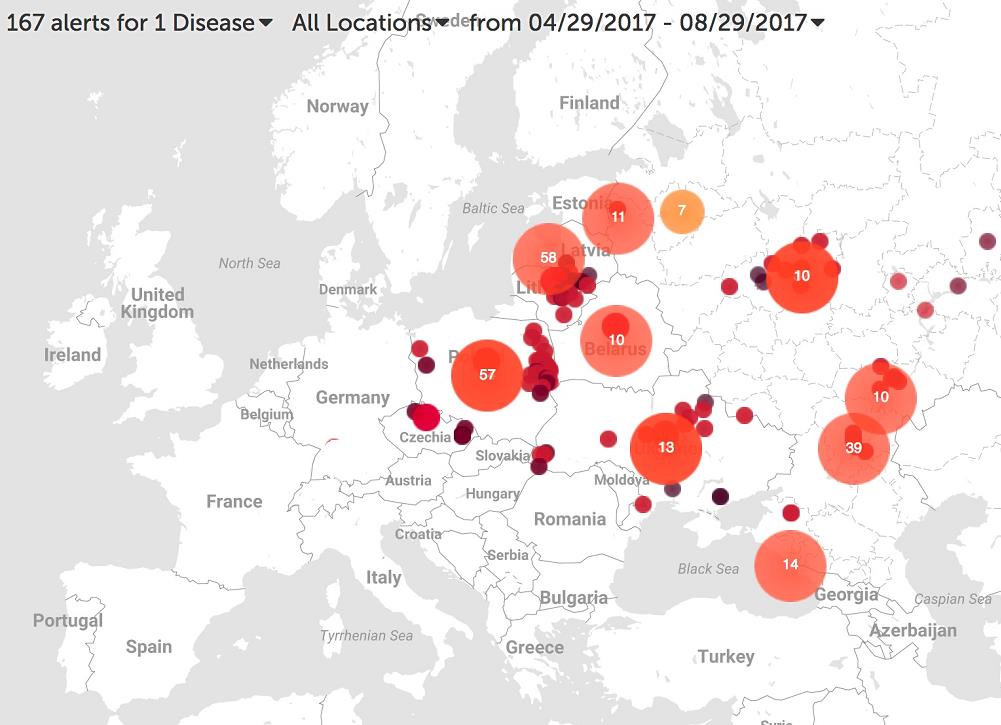
Desafortunadamente, la negligencia con que se ha tratado la PPA en Africa desde su origen por todos y cada uno de los actores implicados en la lucha contra la PPA, contribuyó a que en el año 2007, solamente una década después de su erradicación en la Península Ibérica, el VPPA llegara nuevamente a Europa procedente de África. En esta ocasión, el virus desembarcó en la ciudad de Poti en Georgia, a orillas del mar Negro. El virus llegó de nuevo como lo había hecho 50 años atrás, a través de productos porcinos infectados procedentes de África, donde a día de hoy la enfermedad continúa siendo endémica en muchas regiones, contribuyendo a la pobreza de la zona. Desde que el VPPA llegó al continente europeo se ha expandido de forma descontrolada afectando a países como Rusia, Lituania, Letonia, Estonia y Polonia, entrando por primera vez en la UE en el año 2014. En el mapa adjunto se muestran los casos de PPA detectados en cerdos y jabalíes en los 4 últimos meses en Europa PPA ya confirmados por la FAO (Food and Agriculture Organization).
Han pasado diez años desde el desembarco del VPPA en 2007, la situación continua fuera de control y la necesidad de una vacuna frente a la enfermedad se hace cada vez más evidente.
A diferencia de lo que ocurre actualmente en Europa, donde el virus circula principalmente entre los cerdos domésticos y los jabalíes, la situación en África resulta mucho más compleja. El cerdo doméstico europeo es el único huésped susceptible a la enfermedad en África y el virus se mantiene en un ciclo silvestre entre cerdos salvajes y garrapatas. Los suidos salvajes africanos pueden estar infectados de por vida sin mostrar signos de la enfermedad resultando fundamental en el ciclo, las garrapatas del género Ornithodoros, que facilitan la transmisión ente los suidos salvajes y también al cerdo doméstico. A día de hoy se considera que la PPA es el factor de riesgo más limitante para el crecimiento sostenido de una industria porcina en clara expansión en muchas zonas del continente Africano, contribuyendo así a aumentar la pobreza en una de las áreas ya de por sí más castigadas del planeta.
En el laboratorio liderado por Dr. Fernando Rodríguez en el IRTA-CReSA trabajamos para encontrar una vacuna que ayude a mejorar la situación actual de esta enfermedad porcina que, además, genera tantas perdidas económicas en los países que la padecen. Las instalaciones de bioseguridad de nivel 3+ (BSL-3+) disponibles en el IRTA-CReSA nos permiten trabajar de forma segura con el virus además de poder vacunar e infectar animales con el VPPA, un agente infeccioso con requerimientos trabajo especialmente estrictos en el plano de la bioseguridad.
En el trabajo publicado recientemente en la revista Journal of Virology, se presentan los avances obtenidos durante la Tesis Doctoral de la Dr. Paula L. Monteagudo en el campo de las vacunas frente a la PPA. El trabajo fue realizado bajo la dirección del propio Dr. Fernando Rodríguez en el IRTA-CReSA y la Dra. María Luisa Salas en el Centro de Biología Molecular Severo Ochoa de Madrid, con la colaboración inestimable del Boehringer Ingelheim Veterinary Research Center GmbH & Co. KG, Hannover, Germany.
Monteagudo PL, Lacasta A, López E, Bosch L, Collado J, Pina-Pedrero S, Correa-Fiz F, Accensi F, Navas MJ, Vidal E, Bustos MJ, Rodríguez JM, Gallei A, Nikolin V, Salas ML, Rodríguez F. 2017. BA71ΔCD2: A new recombinant live attenuated African swine fever virus with cross-protective capabilities. J Virol JVI.01058-17 (Para descargar el pdf del artículo)
En este artículo describimos como hemos modificado una cepa virulenta del VPPA aislada en Badajoz en 1971 (BA71), mediante la eliminación específica de un único gen, la hemaglutinina viral, transformándolo en un virus atenuado (BA71∆CD2) que puede utilizarse para vacunar y proteger a los cerdos, de forma experimental, tanto frente a la cepa virulenta de la que procede (virus parental), como frente a otras cepas del VPPA diferentes.
El hecho de que un virus atenuado confiera protección frente a la infección con el virus del que procede no es algo novedoso y hay numerosos trabajos publicados donde se consigue esta protección frente a estas cepas que denominamos como homólogas. Lo novedoso de nuestro trabajo es que utilizando una dosis adecuada del virus atenuado BA71∆CD2 hemos sido capaces de proteger a los cerdos de una forma 100% efectiva frente a un virus coetáneo del BA71, el E75 (España 1975), que por trabajos anteriores realizados en nuestro laboratorio sabemos que es un virus no homólogo o heterólogo (Para descargar el pdf del artículo).
Gracias a este estudio sabemos también que, la protección conferida es dependiente de la dosis utilizada y, que la protección cruzada obtenida in vivo entre las diferentes cepas correlaciona con la habilidad que tiene nuestro candidato vacunal BA71∆CD2 de inducir células T-CD8+ capaces de reconocer ambas cepas, BA71 y E75 in vitro.
Con estos buenos resultados en la mano, quisimos avanzar un paso más y averiguar si nuestro candidato vacunal BA71∆CD2 era capaz de proteger a los animales frente a una infección con la cepa que está actualmente circulando en Europa, la denominada Georgia 2007/01. Esta es una cepa mucho más distante filogenéticamente hablando de BA71 de lo que lo es E75, perteneciendo incluso a un genotipo diferente. Los resultados obtenidos de este experimento fueron impresionantes, pues todos los animales que recibieron la dosis adecuada de BA71∆CD2 sobrevivieron a la infección con la cepa heteróloga altamente virulenta Georgia 2007/01.
Los resultados aquí obtenidos van más allá de poder demostrar una protección frente a Georgia 2007/01, frente a la que ya comienzan a aparecer otros prototipos experimentales, sino que abren la posibilidad de poder proteger frente a virus muy distintos con una sóla vacuna, algo esencial sobre todo pensando en aquellas zonas endémicas en las que hay muchos virus diferente circulando al mismo tiempo, como ocurre en muchas zonas del Africa subsahariana.
El hecho de que BA71∆CD2 se pueda producir en una línea celular estable (COS-1) en lugar de en macrófagos primarios como hasta ahora, abre además la posibilidad de una futura explotación comercial. La ausencia de la hemaglutinina del virus dificulta, por un lado, la transmisión por garrapata del BA71∆CD2, ya que esta proteína es un factor clave para ello y por el otro, permite diferenciar a los animales vacunados de los infectados mediante un sencillo ensayo de inhibición de la hemaglutinación y/o de hemadsorción.
A pesar de los buenos resultados obtenidos, algunos de los animales vacunados mostraron ciertos niveles transitorios de virus en sangre y en secreciones nasales, impidiendo asegurar al 100% su inocuidad en campañas masivas de vacunación en el campo. Así pues, nuestro reto principal se centra ahora en intentar mejorar la bioseguridad de nuestra vacuna y en paralelo, mejorar los métodos diagnósticos que hagan posible diferenciar con facilidad a los animales que han sido vacunados de los que se han infectado de forma natural (DIVA: Differentiating Infected from Vaccinated Animals).
Para contactar con los autores del trabajo, dirigirse a la dirección de correo electrónico: fernando.rodriguez@irta.cat
Agradecimientos: Estos estudios han sido financiados por el Ministerio de Economía y Competitividad (MINECO), gracias a la concesión de una beca FPI (Paula L Monteagudo) y de los Proyectos: AGL2013-48998-C2-1-R, AGL2013-48998-C2-2-R, AGL2016-78160-C2-1-R. Queremos agradecer la financiación adicional recibida Boehringer Ingelheim Veterinary Research Center GmbH & Co. KG, Hannover, Germany¸ sin la cual este trabajo no habría sido posible.