Modelos animales de la condición post-COVID-19

Ahora que la fase de emergencia de la pandemia de COVID-19 ha terminado oficialmente, nos queda enfrentarnos a sus consecuencias a largo plazo.
Alrededor del 40% de los pacientes que tuvieron COVID-19 en los últimos tres años han experimentado síntomas meses después de la infección. Esta sintomatología fue definida inicialmente como COVID persistente por los pacientes -los primeros en llamar la atención sobre sus síntomas de larga duración utilizando las redes sociales- y ahora se conoce como condición post-COVID-19 (PCC).
Los síntomas más comunes de la COVID persistente son fatiga, dificultad para respirar, dolor, aumento del ritmo cardíaco, alteración del sentido del gusto y del olfato, dolor de cabeza y una larga lista de trastornos neurológicos y psicológicos. Los pacientes suelen describir sus dificultades de concentración y memoria a corto plazo utilizando la contundente expresión «niebla mental»; los trastornos del sueño, la ansiedad y la depresión también son quejas frecuentes.
Estos síntomas pueden persistir tras la infección aguda (con pruebas COVID-19 ya negativas) o desarrollarse semanas después del final de la enfermedad, aunque ésta haya sido leve. Dados los cientos de miles de individuos que se han infectado por el SARS-CoV-2 hasta ahora, el número de personas en riesgo de sufrir consecuencias a largo plazo es muy elevado. La PCC representa, por tanto, no sólo una carga sanitaria, sino también un problema social, ya que afecta gravemente a la calidad de vida, reduciendo la capacidad de trabajar y participar en actividades sociales. Curiosamente, la PCC es más frecuente en las mujeres, mientras que las probabilidades de padecer COVID-19 aguda grave son mayores en los hombres.
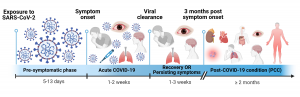
Fig. 1 | Cronología de COVID-19 aguda y PCC en humanos.
Las causas y los mecanismos de la PCC aún no se han caracterizado a nivel molecular, lo que deja a los pacientes que sufren esta enfermedad sin un tratamiento adecuado. El estudio de modelos animales, extremadamente útiles para comprender la COVID-19 aguda y ensayar vacunas y tratamientos, está ayudando a desvelar algunos de los aspectos de la PCC. Hasta la fecha, ningún modelo animal reproduce plenamente la PCC tal y como ocurre en humanos, pero varios estudios realizados en diferentes especies han arrojado resultados interesantes.
Nuestro grupo ha publicado recientemente un artículo en Lab Animal en el que se resumen los conocimientos actuales sobre este tema, centrándose en las manifestaciones neurológicas del PCC, y se discute la aplicabilidad de los modelos animales existentes para comprender mejor sus mecanismos moleculares y celulares.
Por ejemplo, los hámsters se han utilizado ampliamente como modelos para la COVID-19. Se ha descubierto que los hámsters infectados por el SARS-CoV-2 tenían una expresión modificada de genes específicos en el cerebro un mes después de la infección, cuando el virus ya no era detectable en el organismo. Los genes más expresados en estos animales que en los hámsters que nunca fueron infectados por el SARS-CoV-2 se activan normalmente durante la inflamación. Otro estudio ha encontrado inflamación y acumulación de formas alteradas de dos proteínas llamadas tau y alfa-sinucleína en el cerebro de hámsters dos semanas después de la infección por SARS-CoV-2. Estos resultados son especialmente interesantes porque la acumulación de tau y alfa-sinucleína modificadas son hallazgos característicos en el cerebro de pacientes con enfermedades neurodegenerativas (como Parkinson y Alzheimer), lo que sugiere mecanismos similares entre la PCC y estas enfermedades.
Además, los estudios de comportamiento han demostrado que los hámsters infectados presentan una reducción de las actividades espontáneas y un aumento de la sensibilidad al dolor, lo que se asemeja a algunos de los síntomas neurológicos declarados por los pacientes, probablemente debido a una inflamación continua del sistema nervioso.
Estudios similares en ratones han encontrado inflamación a largo plazo en el cerebro tras la infección con SARS-CoV-2, incluso cuando la enfermedad respiratoria era leve y el virus no era detectable en el cerebro. Una vez más, la inflamación iba acompañada de una expresión génica alterada que sugería un deterioro cognitivo como en el envejecimiento y el Alzheimer.
Es importante señalar que la mayoría de los estudios publicados hasta ahora se refieren a animales no vacunados infectados con la cepa original del SARS-CoV-2, pero desde el inicio de la pandemia han aparecido varias variantes, y un número creciente de personas se ha vacunado en todo el mundo, lo que ha mejorado nuestra capacidad para combatir la infección.
Esto plantea dos cuestiones importantes:
1) ¿Influyen las diferencias entre variantes en la probabilidad de desarrollar PCC y en la intensidad de los síntomas?
2) Dado que la PCC puede seguir produciéndose en caso de infección tras la vacunación, ¿es sustancialmente diferente de la enfermedad desarrollada por individuos no vacunados?
Para comprender realmente cómo abordar el problema de la infección prolongada, será necesario más de un modelo animal, con diferentes combinaciones de variantes, estado de vacunación y características genéticas.
No es una tarea fácil: con tantos factores a tener en cuenta y una gama tan amplia de posibles resultados, se necesitarán experimentos complejos.
Junto con los demás miembros del proyecto EPIVINF, financiado por la UE, estamos trabajando para comprender un aspecto específico de la PCC: el impacto del SARS-CoV-2 en la regulación de la expresión génica del huésped y cómo puede afectar a la salud neurológica a largo plazo.
Nuestro artículo: Animal models to study the neurological manifestations of the post-COVID-19 condition | Lab Animal (nature.com)
Página web del proyecto EPIVINF: EPIVINF – Understanding the epigenetic regulation to fight viral infections
Imagen de portada: Imagen de pch.vector en Freepik













